Cyanin3-Maleimid
| Artikel-Nr. | Packungseinheit | Preis | Vorlaufzeit | Jetzt kaufen |
|---|---|---|---|---|
| 11080 | 1 mg |
$125.00
|
Auf Lager | |
| 21080 | 5 mg |
$224.00
|
Auf Lager | |
| 41080 | 25 mg |
$449.00
|
Auf Lager | |
| 51080 | 50 mg |
$895.00
|
Auf Lager | |
| 61080 | 100 mg |
$1490.00
|
Auf Lager |

Thiol-reaktiver Cyanin3-Farbstoff, ein Analogon zu Cy3®-maleimid. Dieses Reagenz kann verwendet werden, um Cyanin3-Fluorophore an Proteine und Peptide, die Cysteinreste enthalten, sowie an andere thiolhaltige Moleküle (wie zum Beispiel thiolhaltige Oligonukleotide) zu binden.
Cystine müssen vor der Markierung mit TCEP (Tris-Carboxyethylphosphin) reduziert werden.
Die Markierung mit Cyanin3-Maleimid ist selektiv und effizient.
Für die Markierung von Antikörpern und anderen sensiblen Proteinen empfehlen wir den Einsatz des wasserlöslichen Sulfo-Cyanin3-Maleimids.
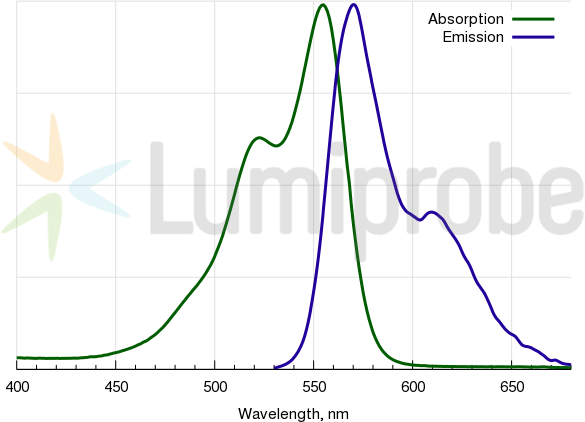
Absorptions- und Emissionsspektren von Cyanin 3
Empfohlenes Protokoll
Rechner
Kunden kauften zusammen mit diesem Produkt
Allgemeine Eigenschaften
| Erscheinungsform: | rotes Pulver |
| Molekülmasse: | 666.56 |
| Molekülformel: | C36H43N4O3BF4 |
| Löslichkeit: | löslich in DMSO(0.50 M = 330 g/L), DMF, Dichlormethan, geringe Löslichkeit in Wasser (0.57 mM = 420 mg/L) |
| Qualitätskontrolle: | NMR 1H, HPLC-MS (95 %) |
| Lagerungsbedingungen: | Lagerbeständigkeit: 24 Monate ab dem Wareneingang bei −20 °C an einem lichtgeschützten Ort. Transport: bei Raumtemperatur bis zu drei Wochen. Längere Lichteinwirkung vermeiden. Trocken lagern. |
| Sicherheitsdatenblatt: | herunterladen |
| Product specifications |
Spektrale Eigenschaften
| Anregungs-/Absorptionsmaximum / nm: | 555 |
|
ε |
150000 |
| Emissionsmaximum / nm: | 570 |
| Fluoreszenz-Quantenausbeute: | 0.31 |
| CF260: | 0.04 |
| CF280: | 0.09 |
Zitierungen
- He, Y.; Zalenski, N.; Stephenson, A. A.; Raper, A. T.; Ghimire, C.; Suo, Z. Conformational Transitions of Streptococcus Pyogenes Cas9 Induced by Salt and Single-Guide RNA Binding. Journal of Biological Chemistry, 2025, 301(2), 108120. doi: 10.1016/j.jbc.2024.108120
- Iudin, D.; Gerridzen, L. J. J. A.; N. Bernal, P.; Schuurmans, C. C. L.; Neumann, M.; Nguyen, L.; van Steenbergen, M. J.; Hak, J.; Li, W.; Casadidio, C.; van Genderen, A. M.; Masereeuw, R.; Levato, R.; Zhang, Y. S.; van Ravensteijn, B. G. P.; Vermonden, T. In-Depth Investigation of Electrostatic Interaction-Based Hydrogel Shrinking for Volumetric Printing and Tissue Engineering Applications. Biomacromolecules, 2025, 26(7), 4108–4123. doi: 10.1021/acs.biomac.5c00117
- Burgos-Bravo, F.; Tong, A. B.; Li, C.; Díaz-Celis, C.; Kaplan, C. D.; LeRoy, G.; Reinberg, D.; Bustamante, C. FACT Weakens the Nucleosomal Barrier to Transcription and Preserves Its Integrity by Forming a Hexasome-like Intermediate. Molecular Cell, 2025, 85(11), 2097-2109.e8. doi: 10.1016/j.molcel.2025.05.002
- Fischer, J.M.; Stewart, M.; Dai, M.; Drennan, S.; Holland, S.; Quentel, A.; Sabuncu, S.; Kingston, B.R.; Dengos, I.; Xiang, L.; Bonic, K.; Goncalves, F.; Yi, X.; Ranganathan, S.; Branchaud, B.P.; Muldoon, L.L.; Barajas, R.F.; Yildirim, A. Peptide Amphiphiles Hitchhike on Endogenous Biomolecules for Enhanced Cancer Imaging and Therapy. bioRxiv, 2024, preprint. doi: 10.1101/2024.02.21.580762






















 $
$ 
